en
names in breadcrumbs

Chrysochromulina ist eine Gattung von Haptophyten. Dieses Phytoplankton ist weltweit in Brack- und Meeresgewässern mit ca. 60 bekannten Arten (Spezies) verbreitet.[2][3] Alle Chrysochromulina-Arten sind phototroph, einige haben sich jedoch als mixotroph erwiesen und zeigen unter bestimmten Umweltbedingungen auch Phagotrophie.[3] Die Chrysochromulina-Zellen sind klein und werden typischerweise mit Hilfe der Elektronenmikroskopie beobachtet. Sie zeichnen sich durch Schuppen (englisch scales) aus.[2][3] Bei einigen Arten wurde nachgewiesen, dass sie unter bestimmten Umweltbedingungen toxische Verbindungen produzieren, die für größere Meereslebewesen einschließlich Fischen schädlich sind.[2][3][4]
Die Individuen der Gattung sind, je nach Art (Spezies) zwischen 3,0 und 13,0 µm groß, wobei die größten Exemplare bei der Art C. polylepis zu finden sind.[2] Die Zelloberfläche ist mit plättchenförmigen Schuppen bedeckt, wobei oft zusätzliche Lagen verschiedener Schuppentypen übereinander liegen.[2]
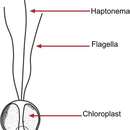
Wie für alle Haptophyten charakteristisch, besitzen die Mitglieder der Gattung Chrysochromulina zwei Geißeln und ein einzigartiges geißelähnliches Organell, das als Haptonema bezeichnet wird.[5] Es gibt (zumindest für einige Arten) auch ein amöboides Stadium ohne Geißeln und Haptonema.[6]
Die Haptonema kann in ihrer Länge stark variieren und dabei bis zu 60 µm erreichen.[2] Sie unterscheidet sich von den Geißeln in Bezug auf die Anordnung der Mikrotubuli. Ihre Funktion ist die der Zellanhaftung und Nahrungsaufnahme.[5]
Haptophyten haben eine Evolutionsgeschichte von etwa 1,2 Milliarden Jahren, Belege aus Mikrofossilien unterstützen diese Ansicht.[7]
Im Jahr 2014 wurde der Entwurf der Genomsequenz von C. tobinii von Forschern der University of Washington veröffentlicht.[7][8] Es war das erste vollständig sequenzierte Genom eines Mitglied der Ordnung Prymnesiales. Man erhofft sich davon ein breites Verständnis der Evolutionsgeschichte der Haptophyten und der Diversität dieser Algenklade. Darüber hinaus kann dies bei der Erforschung bestimmter Gene und Proteine helfen, die für die Bildung von Toxinen und die Freisetzung anderer Chemikalien verantwortlich sind.[8]
Viele früher zur Gattung Chrysochromulina gestellte Spezies werden inzwischen den Gattungen Haptolina oder Prymnesium zugeordnet. Aktuell gehören damit (noch) zur Gattung Chrysochromulina folgende Spezies:[9][10][11][12][13]
Gattung Chrysochromulina Lackey, 1939
unsichere Mitglieder:
bisher lediglich vorgeschlagene Mitglieder:
Neu der Gattung Haptolina zugeordnet (nach WoRMS):
Neu der Gattung Prymnesium zugeordnet (nach WoRMS):
Chrysochromulina spielt eine wesentliche Rolle bei der globalen Kohlenstoffbindung und der Bildung toxischer Algenblüten in den Weltmeeren. Die meisten Haptophyten sind photosynthetische Mikroalgen, aber einige von ihnen sind mixotroph.[7] Haptophyten können sowohl in Süß- als auch in Meerwassersystemen leben. Diese kombinierte Lebensweise macht Haptophyten zu effizienten Organismen in der globalen Kohlenstofffixierung, sie nehmen 30 bis 50 % der photosynthetischen Biomasse im Ozean ein.[17]
Einige Arten, wie z. B. C. polylepis, produzieren ein kohlenstoffreiches, membranschädigendes Toxin.[4] Studien legen einen Zusammenhang zwischen der Stickstoff- und Phosphor-Zusammensetzung in der marinen Umgebung und der Toxinproduktion dieser Haptophyten nahe. Nach früheren Aufzeichnungen fielen hohe Nitratwerte in Kombination mit einer niedrigen Phosphorkonzentration zusammen mit einem Anstieg der Toxizität während Algenblüten.[18] Weitere Forschungen haben inzwischen ergeben, dass sowohl niedrige Stickstoff- als auch niedrige Phosphorwerte in den Zellen zu einem Anstieg der Toxinproduktion führen können, wobei sich Phosphor als die etwas einflussreichere Komponente erwies.[4]
Trotz dieser Korrelation ist es unwahrscheinlich, dass Stickstoff oder Phosphor in direktem Zusammenhang mit der Toxinbildung stehen, da die Toxine selbst stark kohlenstoffbasiert sind. Darüber hinaus sind auch andere wachstumsbegrenzende Faktoren wie Licht und Salzgehalt dafür bekannt, die Toxizität zu erhöhen, was darauf hindeutet, dass die Toxine in Zeiten geringen Wachstums einen selektiven Vorteil für die Verteidigung der Einzeller haben. Studien unterstützen die Idee, dass die Toxinproduktion eine Stoffwechselreaktion auf zellulären Stress aufgrund von Nährstoffeinschränkungen darstellt.[4]
Viele Chrysochromulina-Arten bilden weltweit Algenblüten.[19] Bei einigen dieser Blüten im Nordatlantik können Verbindungen produziert werden, die unter den bestimmten Umweltbedingungen für andere Meeresorganismen giftig sind.[3][19][20] In den skandinavischen Küstengewässern bilden sich die Blüten gewöhnlich zwischen April und August, wobei die spezifischen Chrysochromulina-Arten von Jahr zu Jahr variieren.[3][19]
Im späten Frühjahr 1988 gab es eine Chrysochromulina-Blüte, die sich vom Kattegat bis zum Skagerrak ausbreitete, gebildet nur aus einer einzigen Art, C. polylepis.[19][20] Diese spezielle Blüte war aufgrund der Produktion von hämolytischen Verbindungen durch C. polylepis toxisch für andere Meeresorganismen, einschließlich Protozoen, Wirbellose und 900 Tonnen Zuchtfischen.[19][20]
C. polylepis ist in den in der Region üblichen Konzentrationen normalerweise nicht toxisch. Es wird jedoch angenommen, dass bestimmte Umweltbedingungen wie eine starke Schichtung mit einer warmen Oberflächenschicht und niedrigem Salzgehalt nach einem Winter mit hohen Stickstoffabflüssen, zu einem erhöhten N:P-Verhältnis führten, was dann zu der beobachteten staken Algenblüte führte.[3][19][20]
Es wird auch angenommen, dass die Produktion dieser toxischen Verbindungen das Abweiden von C. polylepis durch Fressfeinde einschränkte, so dass die Blüte von dieser einzigen Art dominiert wurde.[19] Die toxischen Effekte schienen sich später schnell wieder umzukehren und das Nahrungsnetz war bis 1993 dort wiederhergestellt.[19][20]
Von April bis Mai 1992 gab es im südlichen Kattegat eine große Blüte, die aus vielen Phytoplanktonarten bestand, wobei über 90 % der Biomasse Chrysochromulina-Arten waren (allerdings inzwischen z. T. der Gattung Haptolina zugeordnet).[21] Die am häufigsten vorkommenden Arten in der Blüte waren:[21]
C. spinifera, H. hirta und H. ericina zeichnen sich durch relativ kleine Zellen mit langen Dornen aus, die den Gesamtorganismen einen Durchmesser von 25–76 μm verleihen, was für die vorhandenen Ciliaten (als potentielle Fressfeinde) zu groß ist, um sie zu verschlingen; wahrscheinlich ein Grund für den „Erfolg“ der Blüte war.[21]
Es gab keine Beweise, die diese Blüte oder die vorhandenen Arten direkt mit der Produktion von Toxinen (wie bei der C. polylepis-Blüte 1988) in Verbindung brachten.[20][21] Es wurden jedoch etwa 50 Tonnen toter Regenbogenforellen (Oncorhynchus mykiss) in Verbindung mit der Blüte gebracht.[21]
Folgende Viren wurden assoziiert mit Chrysochromulina-Spezies gefunden:
Wegen der Neuzuordnung seines Wirtes zur Gattung Haptolina nicht mehr unter die Chrysochromulina-Parasiten klassifiziert wird der Kandidat
CpV-BQ1 wurde isoliert, indem Süßwasserproben aus dem Ontariosee gefiltert und mittels Transmissionselektronenmikroskopie analysiert analysierte. CpV-BQ1 ist ein ikosaedrisches Virus des Phylums Nucleocytoviricota (NCLDV, nucleocytoplasmic large DNA virus) mit einer Genomgröße von 485 kbp (Kilobasenpaaren). Es ist ein Mitglied der Klasse Megaviricetes (früher vorgeschlagene Ordnung Megavirales) mit Merkmalen der Familien Phycodnaviridae und Mimiviridae. Die Konzentrationen von Chrysochromulina im Ontariosee erwiesen sich als konsistent, während die Konzentrationen von CpV-BQ1 stark variierten.[25]
Chrysochromulina ist eine Gattung von Haptophyten. Dieses Phytoplankton ist weltweit in Brack- und Meeresgewässern mit ca. 60 bekannten Arten (Spezies) verbreitet. Alle Chrysochromulina-Arten sind phototroph, einige haben sich jedoch als mixotroph erwiesen und zeigen unter bestimmten Umweltbedingungen auch Phagotrophie. Die Chrysochromulina-Zellen sind klein und werden typischerweise mit Hilfe der Elektronenmikroskopie beobachtet. Sie zeichnen sich durch Schuppen (englisch scales) aus. Bei einigen Arten wurde nachgewiesen, dass sie unter bestimmten Umweltbedingungen toxische Verbindungen produzieren, die für größere Meereslebewesen einschließlich Fischen schädlich sind.